Special Lecture
Special Lecture - Analysis of Drug-induced Photosensitivity Reactions Reported to the Regional Pharmacovigilance Center of the Korean Pharmaceutical Association
Young Wook Kim, Jung Min Lee, Min Kyung Jung, Sukyeong Kim, and Mo Se Lee*
Regional Pharmacovigilance Center, Korean Pharmaceutical Association, Seoul 06708, Republic of Korea
- 대한약사회 지역의약품안전센터에 보고된 약물유발성 광과민반응 분석
김영욱, 이정민, 정민경, 김수경, 이모세*
대한약사회 지역의약품안전센터
This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Drug-induced photosensitivity is an undesirable effect of topically applied or systemically administrated pharmaceuticals, followed by exposition to sunlight. Photosensitivity reactions are classified into phototoxic and photoallergic reactions. Photosensitivity reactions accounted for a small percentage of total adverse event reports but could significantly impact patients' quality of life if not recognized and managed. We tried to estimate the prevalence and features of drug-induced photosensitivity reactions to understand characteristics for appropriate management. In this article, we analyzed data from the Regional Pharmacovigilance Center of the Korean Pharmaceutical Association(KPA)'s adverse event reporting system to investigate drug-induced photosensitivity reactions from 2013 to 2023. Drug-induced photosensitivity reactions were similarly reported in men and women, and most cases occurred in individuals aged 19 to 65. Symptoms often occurred in spring and summer months when UV radiation is stronger. Various drugs are thought to be related to photosensitivity reactions. Immunosuppressants and NSAIDs are the most frequently reported pharmacological subgroups. Pirfenidone was the most frequently reported chemical substance associated with photosensitivity reactions. Clinical symptoms of photosensitivity reactions included rash, itchiness, and skin discoloration in areas exposed to sunlight. The causality evaluation is categorized as 'possible' or 'probable' indicating a relatively high certainty of the association between the drug and the adverse reaction. While the reported cases to the KPA may not be numerous, these reactions do exhibit gender and seasonal characteristics and are preventable. Therefore patient education and monitoring are needed.
Keywords: photosensitivity, phototoxic, photoallergic, DIP, side effect, adverse effect
광과민반응(photosensitivity)이란 피부가 빛에 비정상적으로 민감하게 되는 현상으로 특정 화학물질과 빛의 상호작용으로 인해 피부 질환이 발생하는 것이다. 햇빛, 인공광(예; 태닝) 등에 의해 유발될 수 있으며 주로 얼굴, 목, 손등, 팔 등 빛에 노출되는 부위에서 발생한다. 이러한 반응은 약물에 의해 촉진될 수 있는데 크림, 연고 등 국소제제 뿐 아니라 경구제, 주사제 등 전신제제에 의해서도 광과민반응이 나타날 수 있다. 주로 자외선을 흡수하는 평면, 삼환계, 다환계 구조를 지닌 약물에서 발생률이 증가하며, 대체로 UVA(320~400 nm) 범위 내의 파장에 의해 유발되는 것으로 알려져 있다.
광과민반응은 광독성(phototoxic)반응과 광알러지성(photoallergic)반응으로 분류된다. 광독성반응은 발생률이 높으며 이론상 약물 또는 방사선량이 일정량 이상 될 경우 누구에게나 발생할 수 있다. 개인의 약물 생체 이용률 및 대사가 다를 수 있으므로 광독성반응에 대한 취약 정도는 달라질 수 있다. 반면 광알러지성반응은 발생률이 낮으며 용량의존적이지 않다.1)
광민감성 약물은 광자(photons)를 흡수하는 외인성 발색단(chromophores)을 가지고 있으며 이발색단의 화학 구조에 따라 흡수하는 방사선의 파장이 결정된다. 대부분의 광과민반응은 UVB보다 UVA에 의해 발생하며 UV는 염증반응(광독성), T세포 매개반응(광알러지)을 유발할 수 있다. 이 두 가지 패턴은 때로 동시에 중복되어 나타날 수 있어 임상적으로 구분이 어려운 편이다.
광독성반응은 국소 및 전신 약물 또는 그 대사체가 빛을 흡수, 직접적인 세포 손상을 유발하며 즉각적으로 나타난다. 광알러지성반응은 약물과 자외선 사이의 상호작용에 의해 피부가 면역반응을 일으킬 때 나타나며 지연된 습진 형태로 나타난다. 광과민반응은 과다색소침착, 가성포르피린증, 광조갑용해증, 발진성 모세혈관확장증, 펠라그라 유사반응, 태선반응, 광분포 다형홍반 및 아급성/만성 피부홍반루푸스 등의 형태로 나타날 수 있다.1,2)
약물유발성 광과민반응은 NSAIDs, 항생제, 이뇨제, 항암제 등 많은 약물에서 나타날 수 있으나 대부분의 경우 기전이 명확하지 않고 인과성을 파악하기 어려워 과소진단, 과소보고되는 경향이 있다. 광과민반응 발생 시 원인을 잘 파악하여 적절한 치료 및 예방을 하는 것이 중요하다. 약물유발성 광과민반응은 햇빛을 피하고 약물을 중단하면 대체로 해소되지만 약물을 중단할 수 없는 경우에는 증상 최소화를 위해 자외선 차단제, 자외선 차단복 등을 사용하거나 국소 스테로이드를 사용한다.3) 약물유발성 광과민반응 발생 위험이 있는 환자는 자외선 차단제, 자외선 차단복, 모자 등을 사용해야 하며, 이때 자외선 차단제는 광범위 스펙트럼으로 차단지수(UPF) 50 이상을 사용하도록 한다. 특히 직업적・환경적 이유로 높은 수준의 일사량에 노출되는 환자는 더욱 주의할 필요가 있다.3,12)
본 연구에서는 2013년부터 2023년까지 대한약사회 이상사례(부작용) 및 환자안전사고 보고 시스템 데이터베이스 자료를 이용, 지역사회에서 실질적으로 나타나고 있는 약물유발성 광과민반응 이상사례의 특성에 대해 알아보고자 하였다. Table 1
|
Table 1 Gender in patients with drug-induced photosensitivity reported to the KPA |
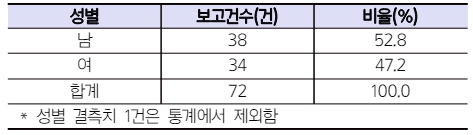
* 성별 결측치 1건은 통계에서 제외함 |
본 연구는 2013년 4월부터 2023년 12월까지 대한약사회 이상사례(부작용) 및 환자안전사고 보고 시스템에 보고된 자료를 이용하였으며 ‘광과민’, ‘광민감’, ‘햇빛’, ‘햇볕’ 등을 키워드로 검색하여 약물유발성 광과민반응 이상사례를 분류하였다. 이 데이터베이스에는 이상사례 보고일자, 이상사례명, 이상사례 증상, 환자의 성별, 연령, 약물의 제품명, 성분명 등이 포함되어 있으며 한 명의 보고자가 복수의 약물을 복용 후 여러 종류의 이상사례를 보고할 수 있으므로 보고건수보다 약물-이상반응의 조합 수가 더 많이 집계된다.
약물유발성 광과민반응 이상사례 보고건에 대해 성별, 연령, 월별로 살펴보았으며 다빈도 보고 성분(ATC Level 3-약물학적 특성별 분류, ATC Level 5-개별 성분명) 및 임상적으로 나타나는 증상과 인과성 평가 결과(WHO-UMC 기준) 등에 대해 살펴보았다.
약물유발성 광과민반응 보고는 총 203,813건 중 73건으로 전체의 약 0.04%를 차지하였다. 약물유발성광과민반응 이상사례의 절대적인 보고건수는 희소한 편이나 해당 이상반응을 인지하지 못할 경우 환자의 삶의 질에 영향을 미칠 수 있으며 예방 가능한 이상반응임에도 적절히 대처하지 못할 수 있다.
약물유발성 광과민반응 보고 환자의 성별은 남성 38명(52.8%), 여성 34명(47.2%)으로 나타났다. 전체보고에서는 남성과 여성의 보고 비율이 각각 32.8%와 67.2%로 여성이 남성보다 약 2배 이상 많았으나4) 약물유발성 광과민반응에서는 전체보고에 비해 상대적으로 남성의 보고가 많은 것이 특징적으로 나타났다.
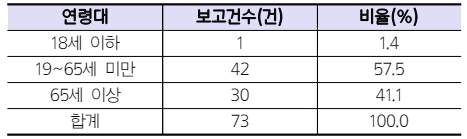
연령별로는 18세 이하 1명(1.4%), 19~65세 미만 42명(57.5%), 65세 이상 30명(41.1%)으로 전체보고와 유사하게4) 19~65세 미만에서 가장 많이 보고되었다. 참고로 18세 이하 보고 1건은 척추염으로 인해 설파살라진, 세레콕시브, 레바미피드, 에페리손 등을 복용한 17세 남성에 의한 것이었다. 이때 의심약물은 설파살라진, 세레콕시브였다.
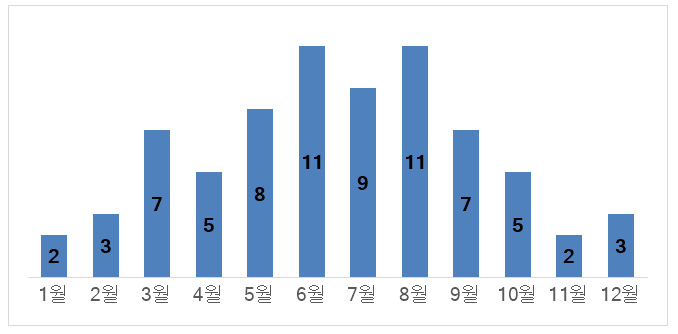
계절적인 발생 빈도를 분석해 본 결과, 73건의 보고 중 여름에 속하는 6월과 8월에 각각 11건으로 가장 많이 보고되었다. 특히 5~8월 4개월 동안 전체 보고의 약 53.4%에 해당하는 39건이 보고되었다.
약물학적 특성별 분류(ATC Level 3)에 의하면 면역억제제, NSAIDs, 고지혈증치료제, 티아지드계이뇨제, 퀴놀론계항생제, 테트라사이클린계 등의 순으로 다빈도 보고되었다. Table 2 Table 3 Table 4
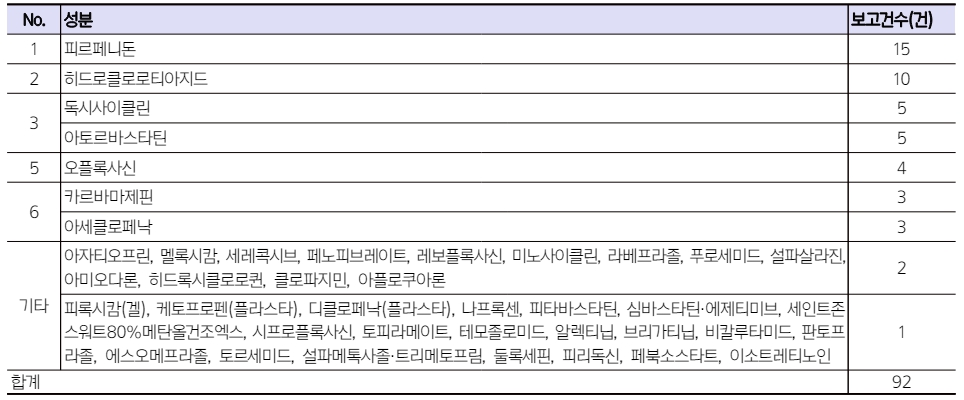
개별 성분(ATC Level 5)으로는 피르페니돈의 보고가 가장 많았으며 히드로클로로티아지드, 독시사이클린, 아토르바스타틴 등이 그 뒤를 이었다. 그 외에 오플록사신, 카르바마제핀, 아세클로페낙 등이 보고되었다.
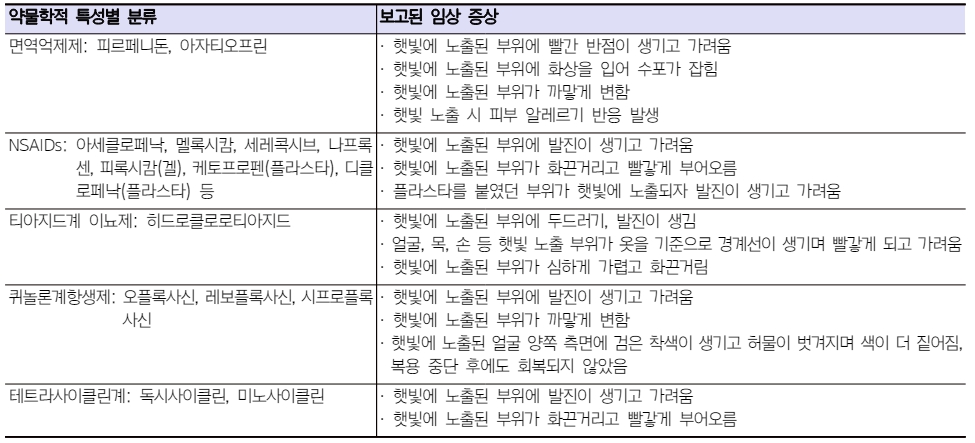
대한약사회에 보고된 약물유발성 광과민반응의 임상 증상은 대체로 유사하게 나타났으며 대표적인 약물학적 특성별 분류에 따라 요약하면 Table 5와 같다. Fig. 1
이러한 증상을 호소한 환자의 대부분에서 처방이 변경되었고 계속 복용해야 하는 경우 자외선 차단제를 꾸준히 사용하도록 권고 받았다.
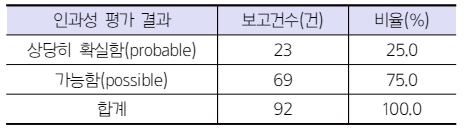
약물유발성 광과민반응의 인과성 평가 결과(WHO-UMC 기준)는 ‘상당히 확실함(probable)’ 25.0%, ‘가능함(possible)’ 75.0%로 나타났다. ‘상당히 확실함’으로 평가된 보고건 중에서는 피르페니돈이 8건으로 가장 많이 보고되었으며 독시사이클린과 카르마바제핀이 각각 2건으로 뒤를 이었다. ‘가능함’으로 평가된 보고건 중에서는 히드로클로로티아지드가 9건, 피르페니돈이 7건, 아토르바스타틴이 5건 보고되었으며 독시사이클린, 아세클로페낙, 오플록사신 등이 3건 보고되었다.
|
Fig. 1 Number of monthly drug-induced photosensitivity reported to the KPA |
|
Table 3 Number of drug-induced photosensitivity reported to the KPA by pharmacological or therapeutic subgroup |
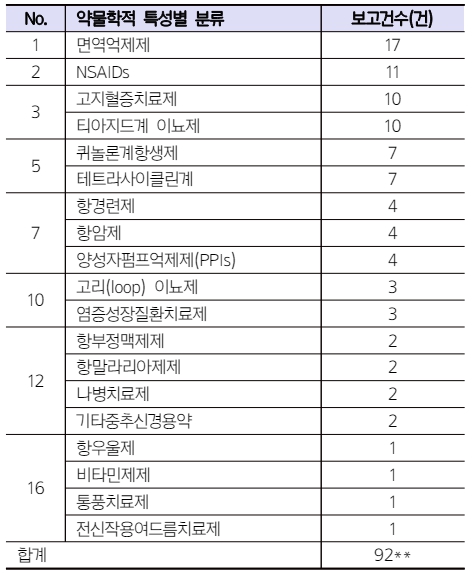
** 약물학적 특성별 분류에 의한 보고건수는 한 명의 보고자가 복 수의 약물 복용 후 이상사례를 보고할 수 있으므로 성별·연령대 별 보고건수의 합계보다 많음 |
|
Table 4 Number of drug-induced photosensitivity reported to the KPA by chemical substance |
|
Table 5 Drug-induced photosensitivity clinical presentation reported to the KPA |
대한약사회 지역의약품안전센터에 보고된 약물유발성 광과민반응은 보고건수가 상대적으로 적은 편에 속하나 발생 가능 약물을 인지하고 예방할 경우 피할 수 있는 이상반응이다. 특히 전체보고에 비해 상대적으로 남성에서 많이 보고되었는데 그 원인에 대해서는 첫째, 남성의 야외활동이 여성보다 많아5) 자외선에 노출되는 빈도가 높기 때문, 둘째, 남성이 여성보다 자외선 차단제 사용에 소홀하기 때문6) 등으로 유추해 볼 수 있다.
약물유발성 광과민반응은 봄-여름에 발생하는 경우가 많은 것으로 알려져 있으며7) 본 연구에서도 자외선이 강한 봄-여름에 많이 보고되었다. 특히 5~8월 4개월 동안 보고된 비율이 전체의 50% 이상을 차지하여 계절별 추이를 확인할 수 있었다. 광과민반응을 유발할 수 있는 약물을 복용할 경우 특히 자외선이 강하고 피부 노출이 많은 봄-여름 외출 시 유의해야 한다.
성분을 살펴보면 알려진 다수의 연구에서 주로 NSAIDs, 항생제, 이뇨제, 항암제 등이 광과민반응 유발성 약물로 제시되고 있으나1) 대한약사회 지역의약품안전센터에 보고된 성분 중에서는 피르페니돈이 가장 많았다는 점이 특징적이다. 피르페니돈은 특발성 폐섬유증(idiopathic pulmonary fibrosis, IPF) 치료에 사용되는 항염증제로서 transforming growth factor(TGF)-8에 의한 섬유아세포의 분화 및 콜라겐 합성을 억제하는 기전의 면역억제제이다. 임상시험에서 중단사유로 광과민반응이 보고된 바 있다.8) 피르페니돈과 위약 투여 시 광민감성 보고가 12% 대 2%로 보고된 연구가 있었으며 또다른 연구에서는 고용량 투여 시 환자의 24%에서 광과민반응이 보고되었다.9) 피부에 존재하는 피르페니돈은 UV 방사선을 흡수하여 지질과산화 및 활성 산소를 발생시켜 피부 병변을 유발한다. 임상 증상은 일광 화상과 유사하며 주로 치료 초기에 발생하고 시간이 지남에 따라 사라지는 경향을 보인다. 그러나 발진이 15일 이상 지속될 경우 용량 감량 또는 투여 중지를 고려해야 한다. 광과민반응이 나타날 수 있는 환자는 빛으로부터 피부를 보호해야 한다. 직접적인 햇빛 노출을 피하고 긴 소매 의류를 입거나 챙이 넓은 모자를 착용하는 것이 좋으며 광범위 자외선 차단제를 사용하도록 한다. 예방조치를 했음에도 불구, 광과민반응이 발생하고 약물 중단이 어려운 경우에는 국소 코르티코스테로이드, 항히스타민제 등으로 치료한다.10)
피르페니돈 외에 NSAIDs, 히드로클로로티아지드, 오플록사신 등 퀴놀론계항생제, 테트라사이클린계 등에서 광과민반응이 보고되었으며 임상 증상은 주로 햇빛에 노출된 부위에 반점, 두드러기, 발진이 생기거나 일광 화상의 형태로 나타났다. 피부가 검게 착색되는 경우도 있었다. Table 6
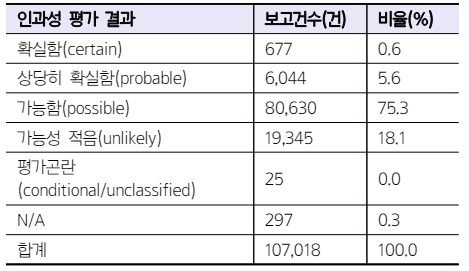
대한약사회 지역의약품안전센터에 보고된 약물유발성 광과민반응의 인과성 평가 결과, ‘상당히 확실함(probable)’이 25.0%, ‘가능함(possible)’이 75.0%로 나타났다. 2023년 한 해 동안 대한약사회 지역의약품안전센터에 보고된 이상사례 22,410건의 약물-이상반응 조합 107,018건에 대한 인과성 평가 결과는 Table 7과 같다.11) 이와 비교하였을 때 약물유발성 광과민반응은 상대적으로 ‘상당히 확실함’의 비율이 높게 나타난 것을 알 수 있다.
인과성 평가에 있어 첫째, 약물투여와 이상사례 발생 간에 시간적 연관성이 있고 둘째, 질병이나 다른 약물에 의한 것으로 보이지 않으며 셋째, 약물 복용을 중단하거나 용량을 감량하였을 때 증상이 호전되는 임상적 변화가 있고 넷째, 재투여 시 임상반응 정보가 없을 때 ‘상당히 확실함’으로 평가할 수 있다. 약물유발성 광과민반응의 경우 환자가 피부 반응 때문에 약물을 중단하는 경우가 많았으며 중단 시 대체로 신속히 회복되는 양상이 관찰되므로 ‘상당히 확실함’의 비율이 높은 것으로 보인다.
|
Table 6 Number of drug-induced photosensitivity reported to the KPA according to WHO-UMC causality assessment system |
|
Table 7 Number of adverse events reported to the KPA in 2023 according to WHO-UMC causality assessment system |
대한약사회 지역의약품안전센터에 보고된 약물유발성 광과민반응은 희소한 편이나 전체 보고에 비해 남성에서의 보고율이 상대적으로 높은 편이었으며 주로 봄-여름철에 보고되는 계절적 특징이 있었다. 또한 상대적으로 인과관계가 높은 것으로 나타났다. 이러한 특성과 피르페니돈, NSAIDs 등 다빈도 보고 약물에 대해 인지할 필요가 있으며, 이를 기반으로 약물유발성 광과민반응 발생 가능성이 높은 환자를 선별, 교육을 통해 이상반응을 예방할 수 있다.
본 연구는 대한약사회 지역의약품안전센터에 보고된 데이터로 분석한 것이므로 우리나라 전체 인구의 특성과는 차이가 있을 수 있다. 그러나 지역사회로부터 실제 보고된 데이터를 분석했다는 데에 의의가 있으며 이후 타기관의 추가적인 연구가 필요할 것으로 사료된다.
- 1. Monteiro, A. F., Rato, M., & Martins, C. (2016). Drug-induced photosensitivity: Photoallergic and phototoxic reactions. Clinics in dermatology, 34(5), 571–581. https://doi.org/10.1016/j. clindermatol.2016.05.006
-

- 2. Liborija Lugovic-Mihic, et al.(2007). Phototoxic and Photoallergic Skin Reactions. Collegium antropologicum 31 Suppl 1:63-7 · February.
- 3. Di Bartolomeo, L., Irrera, N., Campo, G. M., Borgia, F., Motolese, A., Vaccaro, F., Squadrito, F., Altavilla, D., Condorelli, A. G., Motolese, A., & Vaccaro, M. (2022). Drug-Induced Photosensitivity: Clinical Types of Phototoxicity and Photoallergy and Pathogenetic Mechanisms. Frontiers in allergy, 3, 876695. https://doi.org/10.3389/falgy.2022.876695
-

- 4. 대한약사회 지역의약품안전센터 2013~2023년 통계자료
- 5. Paek Kyung Ja, Hwang Young Mi, Lee Jeong Ran. (2013). Actual Wearing Conditions and Attitude: An Initial Report on an Outdoor Wearing Survey for Man and Woman in their 30s to 50s. Fashion & Textile Research Journal Volume 15, Issue5, p787~796.
-

- 6. 대한화장품산업연구원. (2014) 한국인 피부측정, 화장품 이용행태 설문조사. p.21;2015
- 7. Alrashidi, A., Rhodes, L. E., Sharif, J. C. H., Kreeshan, F. C., Farrar, M. D., & Ahad, T. (2020). Systemic drug photosensitivity-Culprits, impact and investigation in 122 patients. Photodermatology, photoimmunology & photomedicine, 36(6), 441–451. https://doi.org/10.1111/phpp.12583
-

- 8. 건강보험심사평가원. (2013). 약제 요양급여의 적정성 평가 결과 pirfenidone 200mg. 서울: 동원.
- 9. Saleem, R., & Vaidya, S. (2021). Pirfenidone-Induced Photosensitive Dermatitis: A Rare Side Effect. Cureus, 13(5), e15200. https://doi.org/10.7759/cureus.15200
-

- 10. Ferrer Guillén, B., Giácaman, M. M., Valenzuela Oñate, C., Magdaleno Tapial, J., Hernández Bel, P., & Pérez Ferriols, A. (2019). Pirfenidone-induced photosensitivity confirmed by pathological phototest. Photodiagnosis and photodynamic therapy, 25, 103–105. https://doi.org/10.1016/j.pdpdt.2018. 11.015
-

- 11. 대한약사회 지역의약품안전센터 2023년 통계자료
- 12. Hofmann, G. A., & Weber, B. (2021). Drug-induced photosensitivity: culprit drugs, potential mechanisms and clinical consequences. Journal der Deutschen Dermatologischen Gesellschaft = Journal of the German Society of Dermatology : JDDG, 19(1), 19–29. https://doi.org/10.1111/ddg.14314
-

 This Article
This Article
-
2024;10(1):16-21
Published on May 31, 2024
- Received on May 7, 2024
- Revised on May 14, 2024
- Accepted on May 17, 2024
 Services
Services
Shared
 Correspondence to
Correspondence to
- Mo Se Lee
-
Regional Pharmacovigilance Center, Korean Pharmaceutical Association 194, Hyoryeong-ro, Seocho-gu, Seoul 06708, Republic of Korea
Tel: +82-2-582-7896, Fax:+82-2-523-7788 - E-mail: iammose@hotmail.com